CORE_REFERENCE // ARTICLE_VIEW
Результаты биологических тестов
lang: ru
MRET-АКТИВИРОВАННАЯ ВОДА И ЕЁ УСПЕШНОЕ ПРИМЕНЕНИЕ ДЛЯ ПРОФИЛАКТИКИ И ПОВЫШЕНИЯ ОПУХОЛЕВОЙ УСТОЙЧИВОСТИ В ОНКОЛОГИИ
Целью данного исследования было изучить на мышах влияние MRET-активированной воды как потенциального средства для профилактики и лечения двух видов онкологических заболеваний (лабораторные модели асцитной опухоли Эрлиха и асцитной формы саркомы). Значительный положительный эффект MRET-активированной воды в отношении опухолевой устойчивости у животных был отмечен в экспериментах на 500 мышах (22 группы по 20 мышей и 10 групп по 5 мышей). Лучшие результаты были получены в группах мышей, получавших MRET-воду, активированную 30 минут (оптимальный режим активации). Существенная противоопухолевая эффективность была подтверждена очень высоким уровнем снижения общего числа жизнеспособных опухолевых клеток на 76% в режиме «профилактического лечения» и на 55% в режиме «терапевтического лечения». Продолжительность жизни мышей, получавших оптимально активированную воду, увеличилась на 61% в режиме «профилактического лечения» и на 43% в режиме «терапевтического лечения». Значительный противоопухолевый эффект MRET-активированной воды у мышей был сопоставим с действием химиотерапевтических препаратов и позволял избежать побочных эффектов, обычно сопровождающих химиотерапию в онкологии.
Рис. 1: Влияние профилактического (1–5) и терапевтического (6–10) применения MRET-активированной воды на среднее общее количество жизнеспособных клеток <C> в асцитной опухоли, полученной у мышей после внутрибрюшинной инокуляции опухолевых клеток карциномы Эрлиха.
Рис. 2: Изменение процента увеличения продолжительности жизни мышей с асцитной карциномой Эрлиха, получавших различные типы MRET-активированной воды в режимах «профилактического лечения» и «терапевтического лечения». Цифры под графиками соответствуют времени активации воды в минутах.
Рис. 3: Влияние MRET-активированной воды на цитотоксическую активность лимфоцитов, содержащих NK-клетки. Активированная вода применялась у мышей без опухолей в двух режимах (21 и 14 дней), называемых «профилактический» (1–5) и «терапевтический» (6–10).
Фото: Внешний вид мышей из групп «контроль» (A) и «профилактического лечения» (оптимальное время активации 30 минут) (B) на 18-й день после инокуляции клеток асцитной карциномы Эрлиха.
Результаты исследования применения воды, активированной неионизирующим процессом молекулярного резонансного эффекта (MRET), для профилактики и повышения устойчивости животных к двум видам онкологических заболеваний in vivo на 500 мышах представлены в данной работе. Исследования физических параметров воды подтвердили, что процесс активации MRET способствует существенной модификации основных физико-молекулярных свойств дистиллированной воды (значительное снижение вязкости как функции приложенного тангенциального давления, а также значительное уменьшение электропроводности и диэлектрической проницаемости как функций частот приложенного электромагнитного поля). Значительный положительный эффект MRET-активированной воды на устойчивость животных к опухолям был отмечен во всех группах мышей на различных фракциях активированной воды. Лучшие результаты были получены в группах мышей, получавших MRET-воду, активированную 30 минут (оптимальный режим активации). Результаты были лучше в режиме «профилактического лечения» по сравнению с режимом «терапевтического лечения». Кроме того, исследование подтвердило, что длительное хранение активированной воды при низкой температуре (около 0°C) в течение 45 дней снижает её противоопухолевую эффективность, но оставляет её на значительно высоком уровне по сравнению с другими фракциями. Результаты тестов показывают двойной механизм действия MRET-воды на опухоли: профилактика и подавление роста опухолей вместе с уменьшением количества жизнеспособных опухолевых клеток. Значительный противоопухолевый эффект MRET-активированной дистиллированной воды у мышей был сопоставим с действием химиотерапевтических препаратов и позволял избежать побочных эффектов, обычно сопровождающих химиотерапию в онкологии.
В ходе исследования цитотоксической активности NK-клеток было отмечено значительное увеличение уровня цитотоксичности лимфоцитов у донорских мышей, получавших MRET-воду, активированную 30 минут. Результаты также показали, что увеличение времени применения MRET-воды с 14 до 21 дня значительно повышает значение индекса цитотоксичности. Можно предположить, что дальнейшее увеличение времени применения MRET-воды приведёт к ещё более высокому уровню активации NK-клеток. Таким образом, применение MRET-активированной воды может быть весьма перспективным подходом для безлекарственной стимуляции иммунных вакцин на основе NK-клеток.
Подробное описание этого исследования представлено в разделе «Преимущества MRET Воды».
_______________________________________________________________________________________________
ВЛИЯНИЕ MRET-АКТИВИРОВАННОЙ СРЕДЫ НА МОРФОЛОГИЮ КЛЕТОК
Исследования in vitro на нормальных клетках PMBC (мононуклеарные клетки периферической крови) и на раковых клетках HeLa (клеточная линия ATCC # CCL-2, аденокарцинома шейки матки) проводились под руководством Патрика Пеццоли, Ph.D., в AltheaDx Technologies, Сан-Диего, США. В экспериментах анализировались: клетки, лизированные в 0 часов, клетки, культивированные 24 часа в необработанной среде, и клетки, культивированные 24 часа в среде, обработанной активатором MRET в течение 30 минут. Образцы ДНК из каждой партии были обработаны, а полученные данные проанализированы с помощью Affymetrix Genotyping Console 3.0 для получения генотипов и числа копий. Подсчёт клеток и процент жизнеспособности определялись методом исключения трипанового синего.
Экспериментальные данные показали отсутствие различий между нулевым часом (контроль), обработанными MRET и необработанными образцами по генотипам и числу копий. Таким образом, активация среды на основе воды методом MRET не вызывала изменений в клетках на генетическом уровне.
Исследования показали, что в среде, активированной методом MRET, жизнеспособность нормальных клеток (PBMC) была выше (Таблица 1), а жизнеспособность раковых клеток (HeLa) была ниже (Таблица 2) по сравнению с их жизнеспособностью в необработанной среде.
Таблица 1: Количество клеток PBMC и % жизнеспособности
| Образец | Количество клеток | % жизнеспособности | Жизнеспособные клетки |
| 0 часов | 3x106 | 92 | 3,27x106 |
| Необработанная | 7x106 | 97 | 6,79x106 |
| Обработанная | 5x106 | 92 | 4,60x106 |
Для нормальных клеток (PBMC) изменения количества клеток были схожи для необработанной и обработанной среды (Рис. 1). Таким образом, обработка методом MRET не влияла на рост нормальных клеток.
Для раковых клеток (HeLa) экспериментальные данные показали значительное подавление роста раковых клеток в среде, обработанной методом MRET. Рост жизнеспособных раковых клеток был подавлен на 54% в среде, обработанной методом MRET, по сравнению с необработанной средой (Рис. 2).
Рис. 1: Количество жизнеспособных клеток PBMC после 24 часов инкубации Рис. 2: Количество жизнеспособных клеток HeLa после 24 часов инкубации
Результаты исследований AltheaDx по раковым клеткам HeLa in vitro подтверждают результаты, полученные ранее в исследовании влияния MRET-воды на устойчивость к опухолям на животных моделях. Исследование на 500 мышах проводилось под руководством профессора В. Высоцкого, С. Олищевского, Ph.D., и Ю. Яниша, Ph.D., в Киевском институте экспериментальной патологии, онкологии и радиобиологии НАН Украины. Было показано существенное подавление роста жизнеспособных опухолевых клеток после употребления MRET-воды. В ходе этого исследования группы мышей в «профилактическом режиме» получали MRET-воду за 2 недели до инокуляции раковых клеток карциномы Эрлиха и в течение 3 недель после инокуляции. Группы мышей в «терапевтическом режиме» получали MRET-воду только в течение 3 недель после инокуляции раковых клеток карциномы Эрлиха. После употребления MRET-воды, активированной 30 минут (оптимальное время активации), рост жизнеспособных опухолевых клеток был подавлен на 76% в «профилактическом режиме» и на 55% в «терапевтическом режиме».
Рис. 1: Количество жизнеспособных клеток PBMC после 24 часов инкубации Рис. 2: Количество жизнеспособных клеток HeLa после 24 часов инкубации
Результаты исследований AltheaDx по раковым клеткам HeLa in vitro подтверждают результаты, полученные ранее в исследовании влияния MRET-воды на устойчивость к опухолям на животных моделях. Исследование на 500 мышах проводилось под руководством профессора В. Высоцкого, С. Олищевского, Ph.D., и Ю. Яниша, Ph.D., в Киевском институте экспериментальной патологии, онкологии и радиобиологии НАН Украины. Было показано существенное подавление роста жизнеспособных опухолевых клеток после употребления MRET-воды. В ходе этого исследования группы мышей в «профилактическом режиме» получали MRET-воду за 2 недели до инокуляции раковых клеток карциномы Эрлиха и в течение 3 недель после инокуляции. Группы мышей в «терапевтическом режиме» получали MRET-воду только в течение 3 недель после инокуляции раковых клеток карциномы Эрлиха. После употребления MRET-воды, активированной 30 минут (оптимальное время активации), рост жизнеспособных опухолевых клеток был подавлен на 76% в «профилактическом режиме» и на 55% в «терапевтическом режиме».
В заключение можно сказать, что исследования, проведённые в AltheaDx Technology, подтвердили, что MRET-активированная вода не влияет на клетки на генетическом уровне; она положительно влияет на морфологию нормальных клеток, повышая их жизнеспособность, и способствует значительному подавлению роста раковых клеток.
_______________________________________________________________________________________________
Восстановительный эффект MRET на количество лейкоцитов
Клиническое наблюдение проводилось у пациента, проходящего химиотерапию по поводу метастатического назофарингеального рака. Обычно количество лейкоцитов (WBC) снижается до очень низкого уровня. Восстановление WBC из этого низкого диапазона обычно занимает около 3–5 недель. Приём MRET-воды предотвратил снижение количества лейкоцитов до минимального уровня и помог восстановить их до предхимиотерапевтического уровня за необычно короткий период — 3 дня.
Таким образом, клиническое наблюдение показало, что на 10-й день после начала химиотерапии (через 3 дня после снижения количества лейкоцитов до 10% от исходного уровня) количество лейкоцитов восстановилось до 93% от исходного уровня. Согласно критериям распределения Стьюдента, восстановление WBC было выше 70% от исходного уровня при p=0,05.
_______________________________________________________________________________________________
АНТИБАКТЕРИАЛЬНЫЙ ЭФФЕКТ MRET-ВОДЫ
Тестирование, проведённое в лаборатории C.A.I. Environmental Laboratory, Карлсбад, США, выявило значительное снижение общего количества колиформных бактерий после процесса активации MRET. В дождевой воде, активированной в течение 30 минут, количество колиформных бактерий уменьшилось на 86% после процесса активации воды. Этот тест подтверждает, что MRET-вода действует как антибактериальный агент, обеспечивая стерилизующий эффект.
_______________________________________________________________________________________________
Влияние MRET-активированной питательной среды на рост Escherichia coli K-12 в аэробных условиях
Исследование выявило значительный эффект MRET-активированной питательной среды в аэробных условиях на процесс роста и размножения микроорганизмов E.coli, их деление, размер колоний и модификацию форм клеток культуры. Было отмечено, что при низкой начальной концентрации клеток исследуемой культуры Escherichia coli K-12 MRET-питательная среда, активированная в течение 30 минут и 60 минут, ингибировала рост культуры соответственно в 27 и 303 раза за 25 часов эксперимента.
Начальный вид чашек Петри с различными фракциями питательной среды в начале эксперимента представлен на Рис. 1.
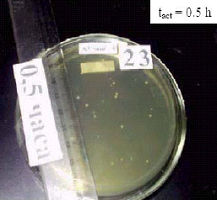
Рис. 1: Чашки Петри в начале эксперимента. Идентичное очень малое количество клеток Escherichia coli K-12 было внесено на поверхность неактивированной питательной среды контрольных чашек и на поверхность чашек с питательной средой, активированной методом MRET в течение 30 и 60 минут (tакт=0,5 ч и tакт=1,0 ч) в аэробных условиях. В начале эксперимента в чашках Петри отсутствуют колонии микроорганизмов.
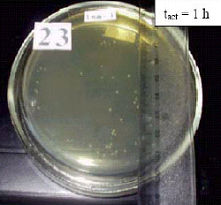
Чашки Петри с выросшими колониями и статистическими параметрами колоний после 23 часов эксперимента представлены на Рис. 2: (a) неактивированная питательная среда (контроль); (b) питательная среда, активированная 30 минут; (c) питательная среда, активированная 60 минут. Чашки Петри после 29 часов эксперимента показаны на Рис. 3. Было выявлено значительное ингибирование роста E.coli в активированных образцах, что подтверждает выраженный бактериостатический эффект MRET-активированной среды.
 |
 |
| (a) Контроль: Количество колоний NC = 1,7x108 КОЕ/мл. Средний диаметр выросших колоний d = 1,1 мм. |
(b) MRET-активированная, tакт = 30 минут: Количество колоний N0,5 = 6,4x106 КОЕ/мл. Средний диаметр выросших колоний d = 1,8 мм. |
 |
|
| (c) MRET-активированная, tакт = 60 минут: Количество колоний N1,0 = 5,2x105 КОЕ/мл. Средний диаметр выросших колоний d = 1,5 мм. |
Рис. 2: Чашки Петри после 23 часов эксперимента. |
|
|
| Рис. 3: Выбранные чашки Петри с выросшими колониями E.coli K-12 после 29 часов эксперимента. |
Этот эксперимент показывает, что процесс активации методом MRET оказывает очень сильный бактериостатический эффект на условно-патогенные микроорганизмы E.coli, и что ингибирование роста E.coli становится более выраженным при увеличении времени активации. Было отмечено, что при низкой начальной концентрации клеток E.coli в питательной среде активация методом MRET в течение 30 минут и 60 минут ингибировала рост культуры соответственно в NC/N0,5 = 27 и NC/N1,0 = 303 раза за 25 часов эксперимента (Рис. 4). Соответственно, уровень бактериостатической активности составил 96% в среде, активированной 30 минут, и 99,7% — в среде, активированной 60 минут. Таким образом, была подтверждена прямая корреляция между бактериостатической активностью MRET-активированной питательной среды и временем активации.
Ингибирование роста бактерий E.coli в аэробных условиях
Рис. 4: Ингибирование роста E.coli в аэробных условиях: 303 раза (tакт=1,0 ч) и 27 раз (tакт=0,5 ч) за 25 часов эксперимента (синий — контроль, красный — 30 минут, зелёный — 60 минут MRET-активированной среды).
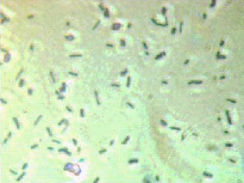
Эксперимент также выявил выраженное влияние MRET-активированной воды на процесс деления микроорганизмов E.coli, модификацию форм клеток культуры и размер колоний. Было отмечено, что одной из причин аномально низкого роста бактерий E.coli связано с модификацией процесса деления клеток в MRET-активированной питательной среде. В процессе роста и размножения большое количество клеток не отделялось друг от друга, и формировались линейные цепочки из 2-3 последовательно соединённых клеток. Клетки культуры, выращенные в неактивированной и MRET-активированной среде, показаны на Рис. 5 и Рис. 6 соответственно.
 |
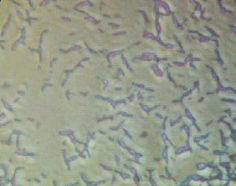 |
| Рис. 5: Клетки Escherichia coli K-12, выращенные в неактивированной среде. | Рис. 6: Клетки Escherichia coli K-12, выращенные в MRET-активированной среде (tакт = 1 час). |
II. Влияние MRET-воды на метаболическую активность бактерий E.coli в аэробных и анаэробных условиях
Восстановительная активность является интегральной характеристикой метаболической активности микроорганизмов и измеряется с помощью цветового индикатора натрия резазурина в процентах степени обесцвечивания (фиолетовый = 0%, красный = 50%, прозрачный = 100%). Восстановительная активность бактерий E.coli снижалась до 3 раз в воде, активированной методом MRET в течение 30 минут, и до 1,6 раз — при активации 60 минут за первые 6 часов эксперимента в аэробных условиях (Рис. 7 и 8).
 |
 |
| K – Контроль; 0,5 – 0,5 часа MRET-активированной воды; 1,0 — 1 час MRET-активированной воды |
|
| RC = 0,2, R0,5 = 0,1, R1,0 = 0,4 K0,5 = 0,5, K1,0 = 2,0 DC = D0,5 = D1,0 |
RC = 25, R0,5 = 9, R1,0 = 19 K0,5 = 0,36, K1,0 = 0,76 DC = D0,5 = D1,0 |
Рис. 7: Сравнительный тест метаболической (восстановительной) активности E.coli (контрольные образцы, 30 и 60 минут MRET-активированной воды) в аэробных условиях: R — восстановительная активность (в контроле, 0,5 часа и 1,0 часа MRET-активированной воды), K — относительная восстановительная активность, D — оптическая плотность.
Относительная восстановительная активность бактерий E.coli в аэробных условиях
Рис. 8: Относительная восстановительная активность E.coli в воде, активированной методом MRET 0,5 часа (K0,5=R0,5/RC — красный цвет) и 1,0 час (K1,0=R1,0/RC — зелёный цвет) по сравнению с контрольными неактивированными образцами (KC=1 — синий цвет) в аэробных условиях.
Этот эксперимент показал, что не существует прямой корреляции между ингибированием метаболической (восстановительной) активности и ингибированием роста E.coli (бактериостатической активностью) в MRET-активированной воде. Бактериостатический эффект существенно выше в воде, активированной 60 минут, а ингибирование восстановительной активности в первые 3 часа выше в воде, активированной 30 минут. Таким образом, этот эксперимент показал, что оптимальное время активации для максимального ингибирования метаболической активности бактерий E.coli в аэробных условиях составляет 30 минут. Такое же оптимальное время активации было выявлено в другом исследовании по применению MRET-активированной воды для профилактики и повышения устойчивости к опухолям in vivo на 500 мышах для двух видов рака, проведённом в Киевском институте экспериментальной патологии, онкологии и радиобиологии НАН Украины.
Учитывая, что небольшая популяция патогенных бактерий, таких как E.coli, обычно присутствует в составе сложных микробных ассоциаций в кишечнике организма, был проведён тест на метаболическую активность бактерий E.coli в анаэробных условиях. Анаэробные условия моделируют среду, аналогичную условиям в кишечнике человека и животных. Исследование показало, что восстановительная активность бактерий E.coli в анаэробных условиях практически не изменялась (Рис. 9 и 10).
K — Контроль; 0,5 — 0,5 часа MRET-активированной воды; 1,0 — 1 час MRET-активированной воды; KSTER — ссылка на стерильность
Рис. 9: Сравнительный тест метаболической (восстановительной) активности E.coli (контрольные образцы, 0,5 часа и 1,0 час MRET-активированной воды, KSTER — ссылка на стерильность) в анаэробных условиях: R — восстановительная активность (в контроле, 0,5 часа и 1,0 часа MRET-активированной воды), K — относительная восстановительная активность, D — оптическая плотность, V — объём газа во флаконах.
Восстановительная активность бактерий E.coli в анаэробных условиях
Рис. 10: Восстановительная активность E.coli в воде, активированной 30 и 60 минут, и в контрольных неактивированных образцах (R0,5 — красный цвет, R1,0 — зелёный цвет, RC — синий цвет) в анаэробных условиях.
Эксперимент показал, что процесс активации методом MRET не оказывает существенного влияния на восстановительную активность бактерий E.coli в анаэробных условиях.
III. Стимулирующий эффект MRET-воды на метаболическую активность сложных микробных ассоциаций в анаэробных условиях
Для моделирования условий, аналогичных условиям в кишечнике человека и животных, был проведён тест на метаболическую активность микробных ассоциаций в анаэробных условиях. Было установлено, что MRET-активированная вода существенно увеличивала восстановительную активность сложных микробных ассоциаций в первые часы эксперимента (Рис. 11).
1,0 — 1 час MRET-активированной воды; 0,5 — 0,5 часа MRET-активированной воды; K — Контроль
Рис. 11: Сравнительный тест метаболической (восстановительной) активности микробных ассоциаций (1,0 час и 0,5 часа MRET-активированной воды и контрольные образцы) в анаэробных условиях: R — восстановительная активность (в контроле, 0,5 часа и 1,0 часа MRET-активированной воды), K — относительная восстановительная активность, V — объём газа во флаконах.
Эксперимент показал, что оптимальное время активации для максимального увеличения метаболической активности микробных ассоциаций в анаэробных условиях составляет 30 минут. Такое же оптимальное время активации было выявлено в процессе ингибирования метаболической активности E.coli в аэробных условиях и в другом исследовании по применению MRET-активированной воды для профилактики и повышения устойчивости к опухолям in vivo.
ВЫВОДЫ
Данное исследование показало, что при низкой начальной концентрации клеток условно-патогенной микробиологической культуры Escherichia coli K-12 в водной питательной среде, активированной 30 минут и 60 минут, рост культуры ингибировался соответственно в 27 и 303 раза за 25 часов эксперимента в аэробных условиях. Эксперимент также выявил выраженное влияние MRET-активированной воды на процесс деления микроорганизмов E.coli, модификацию форм клеток культуры и размер колоний. Было отмечено, что одной из причин аномально низкого роста популяции E.coli связано с модификацией процесса деления клеток в MRET-активированной питательной среде. Эти результаты позволяют предположить, что процесс активации методом MRET и стерилизующий эффект MRET-воды могут быть применены в пищевой промышленности и для очистки воды.
Вторая часть исследования показала, что метаболическая (восстановительная) активность бактерий E.coli снижалась до 3 раз в воде, активированной 30 минут, и до 1,6 раз — при активации 60 минут за первые 6 часов эксперимента в аэробных условиях. Другой эксперимент показал, что процесс активации методом MRET не влияет на восстановительную активность бактерий E.coli в анаэробных условиях и, следовательно, не должен влиять на небольшую популяцию условно-патогенных бактерий, таких как E.coli, обычно присутствующих в микробных ассоциациях в кишечнике организма.
Для моделирования условий, аналогичных условиям в кишечнике человека и животных, был проведён тест на метаболическую активность сложных микробных ассоциаций в анаэробных условиях. Было обнаружено, что процесс активации методом MRET существенно увеличивал восстановительную активность сложных микробных ассоциаций в первые часы эксперимента. Такое же оптимальное время активации — 30 минут — было отмечено в процессе ингибирования метаболической активности условно-патогенных бактерий E.coli в аэробных условиях и для максимального увеличения метаболической активности сложных микробных ассоциаций в анаэробных условиях (характерных для кишечника). Предыдущее исследование по применению MRET-активированной воды для профилактики и повышения устойчивости к опухолям in vivo на 500 мышах также показало лучшие результаты при употреблении воды, активированной 30 минут. Таким образом, данное исследование показывает, что употребление MRET-воды полезно для процесса пищеварения и может способствовать улучшению метаболизма организма.
_______________________________________________________________________________________________
Влияние MRET-активированной воды на стафилококковую инфекцию in vivo на животных (на клетки иммунной системы) и in vitro на культуре Staphylococcus aureus Wood-46
Значительные защитные свойства MRET-воды были подтверждены существенным снижением КОЕ (колониеобразующих единиц) Staphylococcus в гомогенате почек мышей, получавших MRET-воду, по сравнению с контрольной группой после внутрибрюшинного заражения стафилококковой инфекцией через 24 часа. Анализ данных в начале экспериментов позволяет сделать вывод, что значительное снижение колоний патогена в гомогенате почек мышей, получавших MRET-воду, начинается только через 24 часа после инокуляции культуры Staphylococcus. Результаты для воды, активированной 30 минут, были значительно лучше, чем для воды, активированной 15 минут, и все дальнейшие эксперименты проводились с водой, активированной 30 минут.
2. Приём MRET-воды устранил смертность: с 30% (контрольная группа) до 0% (группа MRET) за первые 9 дней эксперимента.
В течение первых 24 часов после внутрибрюшинной инокуляции культуры Staphylococcus не было ни одного случая гибели животных во всех исследуемых группах, что является стандартным результатом. В течение следующих 8 дней в контрольной группе погибло 30% животных, что также является стандартным результатом. Однако в обеих группах мышей, получавших MRET-активированную воду, не было ни одного случая гибели, что является примечательным результатом. Тем не менее, основные последствия стафилококковой инфекции проявляются не в гибели животных, как при онкологических заболеваниях. Вирус Staphylococcus поражает живые системы и органы организма. Эти патогенные микроорганизмы вызывают воспаления, нагноения, абсцессы, фурункулы, ангину, септические состояния и др. Поэтому было проведено детальное исследование процесса стимуляции MRET-водой фагоцитов и лимфоидных органов иммунной системы мышей, инфицированных культурой Staphylococcus aureus, результаты которого представлены в этом отчёте.
3. Развитие локального острого воспаления существенно подавляется при употреблении MRET-активированной воды.
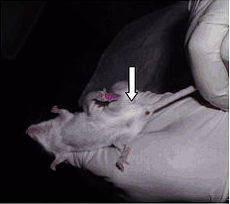
Локальное воспаление вызывалось инъекцией культуры Staphylococcus aureus в заднюю левую лапу. Обычная воспалительная реакция наблюдалась в группе мышей на неактивированной воде: интенсивное покраснение задней левой лапы (Рис. 1). В обеих группах мышей, получавших MRET-воду, не наблюдалось покраснения задней левой лапы после инъекции культуры Staphylococcus (Рис. 2). Результаты этого эксперимента подтверждают факт существенного подавления воспалительной инфекции при регулярном употреблении MRET-воды.
 |
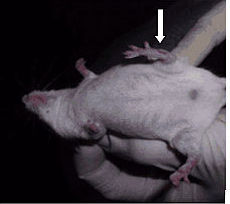 |
| Рис. 1: Вид лап мыши на неактивированной воде (покраснение лапы после инъекции) через 24 часа после инъекции культуры Staphylococcus. | Рис. 2: Вид лап мыши на MRET-активированной воде (отсутствие покраснения лапы после инъекции) через 24 часа после инъекции культуры Staphylococcus. |
4. Приём MRET-воды стимулирует активность фагоцитарной системы и уровень естественной резистентности животных к патогенным микроорганизмам.
В последующих сериях экспериментов инокуляция Staphylococcus aureus Wood-46 проводилась внутрибрюшинно в дозе LD30 для распространения инфекции по всему организму.
Фагоцитарная система — один из основных факторов естественной неспецифической клеточной резистентности к инфекциям и воспалениям. Это первая линия защиты организма от проникновения и размножения патогенных микроорганизмов. Защитная роль фагоцитарных клеток основана на их способности распознавать, поглощать и утилизировать чужеродные агенты, проникшие во внутреннюю среду макроорганизма. Фагоцитоз — основной механизм естественной резистентности, особенно на первой стадии инфекционного процесса; он является регулярной частью формирования специфического иммунного ответа.
Наиболее распространённая методика исследования функциональной активности фагоцитов — определение их фагоцитарной (поглощение чужеродных клеток) и кислородзависимой бактерицидной активности. Фагоцитарная активность нейтрофилов и макрофагов оценивается по Индексу фагоцитоза (процент фагоцитов, поглотивших тест-бактерии) и по Фагоцитарному числу (среднее количество тест-бактерий, поглощённых одним фагоцитом). В качестве тест-бактерий обычно используют культуры Staphylococcus aureus и латекс. Кислородзависимая бактерицидная активность фагоцитов исследуется с помощью NBT-теста: кислородзависимое восстановление нитросинего тетразолия до нерастворимого диформазана производного нитросинего тетразолия фагоцитами. С помощью NBT-теста можно отличить активированные фагоциты от неактивированных.
MRET-вода стимулировала фагоцитарные способности нейтрофилов периферической крови и перитонеальных макрофагов, увеличивая их фагоцитарную активность, в частности Индекс фагоцитоза (Рис. 3А) и Фагоцитарное число (Рис. 3Б). Также наблюдалось повышение их кислородзависимой бактерицидной активности, в частности увеличение количества NBT-положительных фагоцитов (Рис. 4).
Рис. 3А: Индекс фагоцитоза нейтрофилов и макрофагов за две недели эксперимента (объект фагоцитоза — Staphylococcus aureus): 1 — Контрольная группа; 2 — Мыши на MRET-воде (профилактика 4 недели); 3 — Мыши на MRET-воде (профилактика 2 недели).
Рис. 3Б: Фагоцитарное число нейтрофилов и макрофагов за две недели эксперимента (объект фагоцитоза — Staphylococcus aureus): 1 — Контрольная группа; 2 — Мыши на MRET-воде (профилактика 4 недели); 3 — Мыши на MRET-воде (профилактика 2 недели).
Рис. 4: Кислородзависимая бактерицидная активность (NBT-тест) нейтрофилов и макрофагов за две недели эксперимента:
1 — Контрольная группа; 2 — Мыши на MRET-воде (профилактика 4 недели); 3 — Мыши на MRET-воде (профилактика 2 недели).
Эксперименты подтвердили повышение эффективного потенциала фагоцитов, которые составляют один из основных факторов естественной защиты организма и инициируют иммунный ответ.
Анализ данных в начале экспериментов позволяет сделать вывод, что значительные изменения всех исследуемых параметров у мышей на MRET-воде (снижение колоний патогена в гомогенате почек, увеличение массы и клеточности лимфоидных органов, усиление фагоцитарной и бактерицидной активности макрофагов и нейтрофилов) начинаются только через 24 часа после инокуляции культуры Staphylococcus. Иными словами, приём MRET-воды увеличивает потенциал иммунной системы организма для противодействия инфекциям без изменений жизненных параметров иммунных органов и функций до проникновения инфекционных патогенов в организм.
К концу двух недель эксперимента средние значения исследуемых параметров в обеих группах мышей на MRET-воде (профилактика 4 и 2 недели соответственно) значительно увеличились по сравнению с контрольной группой. Различия средних значений исследуемых параметров у групп мышей, получавших MRET-воду, по сравнению с контрольной группой на неактивированной воде были статистически значимыми при p<0,05 (для большинства параметров). Эти результаты подтверждают значительное усиление фагоцитарной активности и иммунного ответа после употребления MRET-воды.
Различия средних значений исследуемых параметров между группами мышей на MRET-воде были статистически незначимыми, что подтверждает схожесть уровня благоприятного эффекта MRET-воды в обеих группах. Этот факт также подтверждает, что регулярное употребление MRET-воды даёт положительный эффект за довольно короткий срок (2 недели на модели лабораторных мышей).
5. Приём MRET-воды существенно усиливает иммунную активность лимфоидных органов.
К концу очередной серии экспериментов в обеих группах мышей на MRET-воде было отмечено существенное статистически значимое (p<0,05) увеличение массы и клеточности (количества клеток) селезёнки и лимфатических узлов, а также незначительное увеличение массы и клеточности тимуса (Рис. 5 и 6).
Рис. 5: Масса лимфоидных органов за две недели эксперимента: 1 — Контрольная группа; 2 — Мыши на MRET-воде (профилактика 4 недели); 3 — Мыши на MRET-воде (профилактика 2 недели).
Рис. 6: Клеточность лимфоидных органов за две недели эксперимента: 1 — Контрольная группа; 2 — Мыши на MRET-воде (профилактика 4 недели); 3 — Мыши на MRET-воде (профилактика 2 недели).
Эти результаты подтверждают факт значительного усиления иммунного ответа у животных на MRET-воде при инфицировании Staphylococcus. Различия исследуемых параметров между группами мышей на MRET-воде (4 недели и 2 недели профилактического приёма) были незначительными, что подтверждает достаточно быстрое проявление положительного эффекта MRET-воды на иммунную активность лимфоидных органов.
В начале эксперимента клеточность и масса лимфоидных органов у групп на MRET-воде не проявляли выраженной тенденции к изменениям. Можно предположить, что приём MRET-воды влияет на массу и клеточность лимфоидных органов только в период инфекции.
ВЫВОДЫ:
Употребление MRET-активированной воды значительно усиливает факторы естественной резистентности организма, которые составляют первую линию защиты от проникновения и размножения патогенных микроорганизмов.
Анализ данных в начале эксперимента позволяет сделать вывод, что значительные изменения всех исследуемых параметров у мышей на MRET-воде (снижение колоний патогена в гомогенате почек, увеличение массы и клеточности лимфоидных органов, усиление фагоцитарной и бактерицидной активности макрофагов и нейтрофилов) начинаются только через 24 часа после инокуляции культуры Staphylococcus. Иными словами, приём MRET-воды увеличивает потенциал иммунной системы организма для противодействия инфекциям без изменений жизненных параметров иммунных органов и функций до проникновения инфекционных патогенов в организм.
К концу двух недель эксперимента средние значения исследуемых параметров в обеих группах мышей на MRET-воде (профилактика 4 и 2 недели соответственно) значительно увеличились по сравнению с контрольной группой. Различия средних значений исследуемых параметров у групп мышей, получавших MRET-воду, по сравнению с контрольной группой на неактивированной воде были статистически значимыми при p<0,05 (для большинства параметров). Эти результаты подтверждают значительное усиление фагоцитарной активности и иммунного ответа после употребления MRET-воды.
Различия средних значений исследуемых параметров между группами мышей на MRET-воде были статистически незначимыми, что подтверждает схожесть уровня благоприятного эффекта MRET-воды в обеих группах. Этот факт также подтверждает, что регулярное употребление MRET-воды даёт положительный эффект за довольно короткий срок (2 недели на модели лабораторных мышей).
II. Влияние активации методом MRET на процесс роста стафилококковой культуры в питательной среде
Следующие эксперименты были направлены на изучение влияния активации методом MRET на процесс роста и развития культуры Staphylococcus aureus Wood-46 in vitro в питательной среде (МПА — мясо-пептонный агар). Бактериальная культура выращивалась до стационарной фазы, затем высевалась на МПА в виде суспензии с разной плотностью инокуляции. МПА с культурой активировали методом MRET в течение разного времени (15, 30, 45 и 60 минут соответственно) с соблюдением требований стерильности. Чашки Петри с активированной и неактивированной средой (МПА с культурой) накрывали стеклянными крышками (аэробные условия) и помещали в термостат для культивирования при температуре 37°C в течение 18–24 часов.
После культивирования наблюдали морфологические и тинкториальные свойства культур и подсчитывали количество выросших колоний на МПА. Бактериостатическая активность MRET-активированной питательной среды (МПА) измерялась как Индекс бактериостатической активности (ИБА). Индекс бактериостатической активности определяется как коэффициент ингибирования роста и размножения патогенов в бактериостатической среде, в частности в MRET-активированной питательной среде. Он рассчитывается как уменьшение количества колоний (КОЕ — колониеобразующие единицы) в MRET-активированной среде по отношению к контрольным образцам, не подвергавшимся активации:
ИБА = (Nконтроль — Nакт)/Nконтроль
где N — количество бактериальных колоний (КОЕ) в контрольной (неактивированной) и MRET-активированной питательной среде соответственно.
где N — количество бактериальных колоний (КОЕ) в контрольной (неактивированной) и MRET-активированной питательной среде соответственно.
Для проверки стерильности экспериментов чашки Петри с питательной средой (МПА) без стафилококковой культуры подвергали процессу активации, а затем выдерживали в термостате. Колонии культуры не обнаруживались, что подтверждает стерильность среды.
РЕЗУЛЬТАТЫ:
В ходе исследования была выявлена прямая корреляция между временем активации (tакт), начальными концентрациями стафилококковой культуры (N0) и количеством колоний, выросших на MRET-активированной среде. Результаты представлены ниже в виде серии фотографий чашек Петри с выросшими колониями на поверхности МПА и соответствующих диаграмм по данным этих экспериментов (Рис. 7–12).
В процессе исследования анализировалось влияние активации методом MRET на рост стафилококковой культуры при достаточно низкой начальной концентрации патогенов. Данные для более высоких начальных концентраций N0 > 103 бактерий/мл не анализировались из-за трудностей подсчёта очень большого количества колоний, несмотря на выраженную бактериостатическую активность MRET-активированной питательной среды при высоких концентрациях.
Был отмечен выраженный бактериостатический эффект 92–93% после активации методом MRET в течение 30 минут и более для культур с начальной концентрацией N0 = 103 бактерий/мл (Рис. 7 и 8) и 70–90% для начальной концентрации N0 = 102 бактерий/мл (Рис. 9 и 10). Для культур с низкой начальной концентрацией N0 = 10 бактерий/мл бактериостатическая активность в среде, активированной 15 минут, превышала 93%, а в среде, активированной 30 минут, наблюдалось 100% ингибирование стафилококковых колоний (Рис. 11 и 12).
.jpg) |
.jpg) |
| N0 = 103 бактерий/мл, Контроль | N0 = 103 бактерий/мл, tакт = 15 мин |
.jpg) |
 |
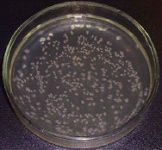
| N0 = 103 бактерий/мл, tакт = 30 мин | N0 = 103 бактерий/мл, tакт = 45 мин |
 |
|
| N0 = 103 бактерий/мл, tакт = 60 мин |
Рис. 7: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 103 бактерий/мл.
Рис. 8: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 103 бактерий/мл. ИБА — индекс бактериостатической активности (уменьшение количества колоний по отношению к контрольным образцам, не подвергавшимся активации).
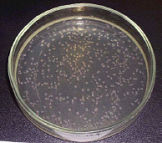 |
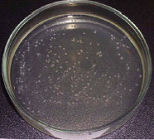 |
| N0 = 102 бактерий/мл, Контроль | N0 = 102 бактерий/мл, tакт = 15 мин |
.jpg) |
.jpg) |
| N0 = 102 бактерий/мл, tакт = 30 мин | N0 = 102 бактерий/мл, tакт = 45 мин |
.jpg) |
|
| N0 = 102 бактерий/мл, tакт = 60 мин |
Рис. 9: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 102 бактерий/мл.
Рис. 10: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 102 бактерий/мл. ИБА — индекс бактериостатической активности (уменьшение количества колоний по отношению к контрольным образцам, не подвергавшимся активации).
 |
 |
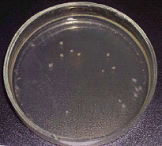
| N0 = 10 бактерий/мл, Контроль | N0 = 10 бактерий/мл, tакт = 15 мин |
Рис. 11: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 10 бактерий/мл.
Рис. 12: Влияние времени активации методом MRET на ингибирование роста культуры Staphylococcus aureus Wood-46 с начальной концентрацией N0 = 10 бактерий/мл. ИБА — индекс бактериостатической активности (уменьшение количества колоний по отношению к контрольным образцам, не подвергавшимся активации).
ВЫВОДЫ:
1. Активация водной питательной среды методом MRET с суспензией стафилококковой культуры приводит к возникновению высокой бактериостатической активности питательной среды, которая зависит от времени активации и начальной концентрации клеток культуры.
2. Бактериостатическая активность увеличивается с увеличением времени активации (изучались времена активации до 60 минут).
3. Эффективность бактериостатической активности возрастает при уменьшении начальной концентрации суспензии стафилококковой культуры. Процесс активации методом MRET наиболее эффективен для суспензий с концентрацией не более 103 бактерий/мл.
4. Результаты исследования свидетельствуют о высокой эффективности активации методом MRET для ингибирования роста колоний и размножения стафилококковых микроорганизмов in vitro. Эти результаты позволяют предположить, что процесс активации методом MRET и стерилизующий эффект MRET-воды могут быть применены в пищевой промышленности и для очистки воды.
_______________________________________________________________________________________________
Анализ живых клеток крови
В данном случае образец крови до приёма активированной воды показывает атаку свободных радикалов на клетки. Обратите внимание на «игольчатые» клетки крови, которые составляют почти 90% препарата. Через 30 минут после приёма активированной воды в образце крови не наблюдается среды свободных радикалов.
В данном случае образец крови до приёма активированной воды показывает так называемое образование рулонов, когда клетки крови выстраиваются стопкой, образуя червеобразный рисунок. Через 30 минут после приёма активированной воды большинство этих структур распалось, образовав отдельные округлые клетки.
_______________________________________________________________________________________________
_______________________________________________________________________________________________
Влияние MRET-воды на прорастание семян и рост растений
Эксперименты по изучению влияния MRET-активированной воды на растения проводились в течение 3 месяцев в Киевском институте генетики растений НАН Украины под руководством проф. В. Высоцкого, Киевский национальный университет. MRET-активированная вода ускоряла процесс прорастания семян ряда растений (в частности, капусты, тыквы, фасоли, редиса и гороха) и способствовала их росту.
